понедельник, 28 апреля 2014 г.
воскресенье, 27 апреля 2014 г.
Именные реакции в органической химии
Именные реакции можно найти во многих справочниках по органической химии,
но я хочу разделить их по классам химических соединений. И, конечно, это далеко
не все именные реакции, это те реакции, которые часто встречаются в школьном
курсе органической химии.
Именные
реакции алканов:
- Реакция Вюрца — «именная» реакция удлинения цепи, а точнее, удвоение количества атомов углерода:
C2H5Cl + 2Na +ClC2H5 → C4H10 + 2NaCl (из этана получили
бутан)
- Реакция Коновалова: c разбавленной азотной кислотой под давлением алканы нитруются:
С2H6 + HNO3 (HO-NO2) → С2H5NO2 + H2O
(нитроэтан)
- Еще одна «именная» реакция: реакция Кольбе: электролиз солей карбоновых кислот:
2СH3COONa -(электролиз)-→ СH3-CH3 (этан) +
2СO2 +2Na
Именные реакции алкенов:
- Присоединение по правилу Марковникова:
водород присоединяется к наиболее
гидрогенезированному (= к тому, у которого больше водородов) атому углерода при
двойной связи:
СH2=CH-CH3 + HCl = CH3-CH2Cl-CH3
- Обратная реакция — дегидрирования - правило Зайцева — водород отнимается от самого ненасыщенного водородами (наименее гидрогенизированного) атома углерода.
Именные реакции алкинов:
- реакция Кучерова
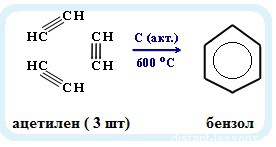
- Реакция Зелинского
Именные реакции аренов:
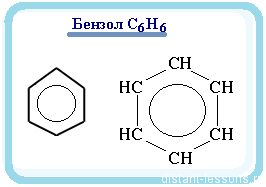
- Ту структурную формулу, которую мы сейчас используем — «скворечник», называют формулой Кекуле:
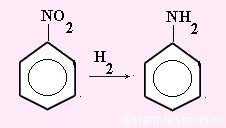
- Реакция Зинина — восстановление нитробензола и его нитрогомологов:
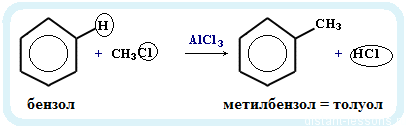
- Реакция Фриделя-Крафтца - алкилирование аренов:
Нуклеиновые кислоты Состав.
Нуклеиновые кислоты
содержатся абсолютно во всех клетках — как у живых организмов, так и у вирусов.
«Нуклео»
— ядро -т.е. это вещества, содержащиеся главным образом в ядрах клеток
эукариотических организмов, но так же могут содержатся и в других
органойдах; в прокариотческих организмах и у вирусов нуклеиновые кислоты
располагаются в цитоплазме.
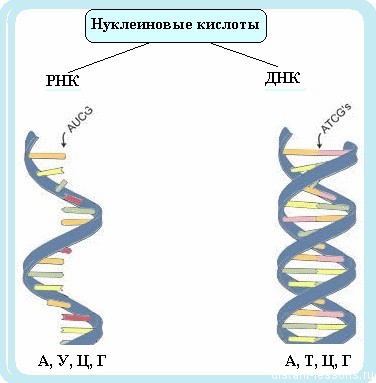
Нуклиновые кислоты бывают
двух типов: ДНК и РНК
РНК — рибонуклеиновая
кислота
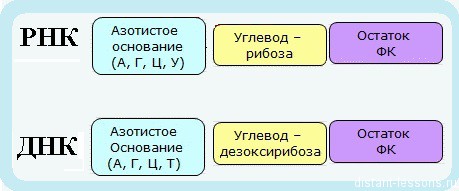
Нуклеотиды — соединения
— азотистые основания — мономеры этих аминокислот
Нуклеотиды ДНК: А — аденин, Т —
тимин, Ц — цитозин, Г — гуанин
Нуклеотиды РНК: А — аденин, У — урацил, Ц — цитозин, Г — гуани
Нуклеотиды РНК: А — аденин, У — урацил, Ц — цитозин, Г — гуани
РНК в отличие от ДНК не имеет тимина
— вместо него стоит нуклеотид урацил — У
Это
первичная структура молекул
Функции нуклеиновых кислот
Генетический код — это последовательность нуклеотидов в молекуле ДНК.
Это основа любого организма, по сути — это информация о самом организме ( как у
любого человека ФИО, идентифицирующее личность- это последовательность букв,
или последовательность цифр — серия паспорта).
Основные функции нуклеиновых кислот —
в хранении, реализации и передаче наследственной информации, «записанной» в
молекулах в виде последовательности определенных нуклеотидов.
·
ДНК отвечает
именно за «идентификацию» и передачу наследственной информации,
·
функции РНК
немного отличаются — она отвечает за производство белка — в организмах —
эукариотах и бактерий и за наследственную информацию — в клетках некоторых вирусов
(РНК-вирусы).
·
По меньшей мере 8
процентов генома человека порождено вирусами, чей генетический код объединился
с нашим в течении около 40 миллионов лет эволюции приматов.
·
Уже сегодня
специалисты могут идентифицировать личность человека по остаткам «ДНК касания»,
которые остались в отпечатках пальцев на месте преступления.
·
Если размотать
ДНК всех клеток вашего тела, то они растянутся на расстояние в 16 миллиардов
километров — это примерно равно расстоянию от Земли до Плутона и
обратно или более 30 раз от Земли до Солнца и обратно.
вторник, 22 апреля 2014 г.
Качественные реакции на белок
Биуретовая Реакция
Ксанторотеиновая реакция- для обнаружения ароматических аминокислот в белках
Ксанторотеиновая реакция- для обнаружения ароматических аминокислот в белках
понедельник, 21 апреля 2014 г.
Структура белка. Свойства белка
Вопросы для актуализация знаний:
- В каких пределах изменяется молекулярная масса белков?
(От нескольких тысяч д - Какие элементы входят в состав белка?
- о нескольких миллионов Mr белка яйца = 36.000, Mr белка мышц = 1.500.000.)
- Кто из ученых предложил пептидную теорию, которая стала ключом к тайне строения белка?
(Русский ученый А.Я. Данилевский, немецкий ученый Э.Г.Фишер.) - В чем суть этой теории?
(Белки – это полимеры, состоящие из остатков аминокислот, соединенных пептидной связью HN–CO.) - Какое еще название белков из этого следует? (Пептиды.)
- На какие группы делят белки по степени сложности?
(Простые – протеины – состоящие только из остатков аминокислот, сложные – протеиды – имеющие еще и небелковый компонент: липопротеиды– кроме белкового компонента содержат липиды, фосфопротеины – содержат фосфорную кислоту.) - Какова структурная организация белков?
(Различают первичную, вторичную, третичную, четвертичную, структуру белков.) - Что представляет первичная структура белка?
(Строго определенная последовательность аминокислотных остатков полипептидной цепи, все связи ковалентные.) - 9) Что представляет вторичная структура белка?
(Белковая макромолекула, свернутая в спираль, между витками которой водородные связи.) - 10) Что такое третичная структура белка?
(Спиралевидная пептидная цепь, уложенная в клубок-глобулу, за счет водородных, гидрофобных, дисульфидных связей.) - 11) Какова четвертичная структура белка?
(Сложный агрегатный комплекс из полипептидных цепей, в котором присутствуют все перечисленные типы связей.)


Белки. История открытия.
Ни в одной области
человеческих знаний не было высказано такого количества гипотез, как в химии
белка.
В 1754 г. итальянский
учёный Я.Б.Беккари опубликовал отчёт о работе, выполненной ы 1728 г. Он выделил
из пшеничной муки клейкую массу - клейковину. Оказалось, что клейковина,
вещество растительного происхождения, напоминала по свойствам продукты, которые
можно было получать из животных организмов. Беккари сделал вывод о
существовании особых веществ, присущих и растениям, и животным. Эта работа
положила начало изучению белков.
В 1888 г. русский учёный
биохимик А.Я.Данилевский на основании своих опытов впервые высказал гипотезу о
пептидной связи между остатками аминокислот в белковой молекуле.
В 1899 г. исследованием
белков занялись немецкие химики-органики Эмиль Фишер и Франц Гофмейстер. Они
высказали предположение: в белках аминокислоты связаны за счёт аминогруппы
одной кислоты и карбоксила другой. При образовании такой связи выделяется
молекула воды.
Эта гипотеза была
блестяще подтверждена экспериментально в 1907 г. и получила название
«полипептидная теория».
Белки – природные
высокомолекулярные соединения (биополимеры), основа всего живого на Земле. Во
всех живых организмах белки играют исключительно важную роль: они участвуют в
построении клеток мышечной и нервной тканей; входят в состав кожи. Все
жизненные процессы в организме осуществляются при участии белков, например с их
помощью кислород доставляется из лёгких в ткани, выводится углекислый газ.
Белки играют в
организме и защитную роль (обеззараживают чужеродные вещества), снабжают его
энергией: при расщеплении 1г белка освобождается 17,6 кДж. Белки-ферменты –
катализаторы многих химических процессов, происходящих в организме. О роли
белков для жизни Ф.Энгельс писал: «Жизнь есть способ существования белковых
тел».
Белки – основной
продукт питания. Средняя потребность человека в белке за сутки составляет
80-100 г. Много белка содержат (в%): икра – 26,7, мясо – 13-14, рыба – 13-18,
горох – 22, кормовые дрожжи – 45.
Подписаться на:
Сообщения (Atom)


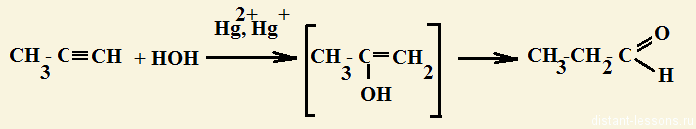






















- Follow Us on Twitter!
- "Join Us on Facebook!
- RSS
Contact